Rôle des lymphocytes T spécifiques des Ag tumoraux dans la réponse clinique aux immunothérapie.
Pr Maha Ayyoub
Des études ancillaires aux essais cliniques d’immunothérapie par anti-PD-1 ont proposé que la présence d’une réponse lymphocytaire T anti-tumorale préalable au traitement soit nécessaire à son efficacité. De plus, l’association observée entre des taux élevés de mutations somatiques tumorales et l’efficacité des anti-PD-1 suggère que ces réponses lymphocytaires T pourraient cibler les néoantigènes codés par ces mutations. Cependant, aucune analyse systématique des lymphocytes T spécifiques des néoantigènes et des autres familles d’antigènes tumoraux n’a été réalisée dans des cohortes de patients recevant des AcM anti-PD-1 ou anti-PD-L1.
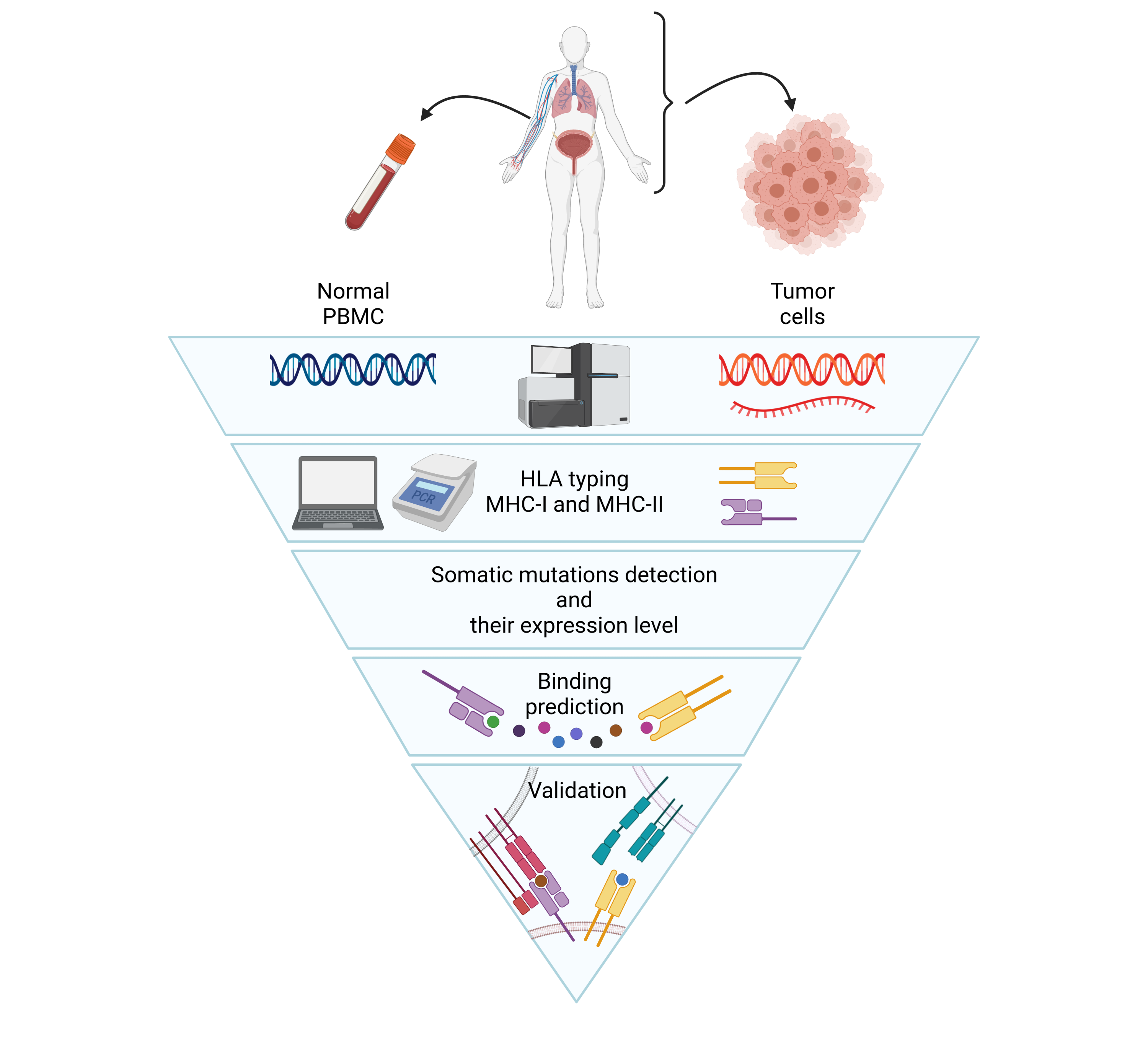
Afin d’étudier le rôle des réponses lymphocytaires T dans la réponse clinique aux immunothérapies, nous nous basons sur trois cohortes prospectives de patients atteints de cancer bronchique, urothélial ou de la sphère ORL et traités par anti-PD-1 ou anti-PD-L1 (protocole MINER, Monitor ImmuNothERapy, NCT03514368). Nous utilisons une approche systémique d’identification des antigènes tumoraux par analyse de l’exome normal et tumoral ainsi que du transcriptome tumoral. Une analyse des réponses T CD8 et CD4 spécifiques de l’ensemble des antigènes exprimés par la tumeur est réalisée de façon personnalisée chez tous les patients. Le phénotype et les fonctions des lymphocytes anti-néoantigènes sont comparés à ceux des lymphocytes T spécifiques des antigènes tumoraux partagés, en particulier ceux du groupe « Cancer testis antigens » dans les trois types tumoraux et les Ag HPV dans les cancers de la tête et du cou HPV-induits. L’évolution de l’ensemble des réponses lymphocytaires T est suivie, pour chaque patient, le long de la thérapie. Les signatures moléculaires des tumeurs sont déterminées par l’analyse des données de transcriptomique et génomique. Finalement, des études de corrélation sont réalisées afin d’investiguer le rôle des réponses immunitaires dans l’évolution de la maladie et la réponse clinique à l’immunothérapie.
Les résultats de ces études participeront à établir les liens mécanistiques entre l’inhibition des points de contrôle immunitaire et le contrôle de la progression tumorale, à définir des biomarqueurs de réponse à ces thérapies et à la conception de thérapies combinées permettant d’augmenter le nombre de patients répondeurs à l’immunothérapie.
Technologies utilisées
Cytométrie en flux (marquages 17 couleurs) ; analyse des lymphocytes T spécifiques de l’antigène par multimères HLA/peptide ; RNASeq, whole exome sequencing ; Analyse bio-informatique ; Analyses fonctionnelles des lymphocytes T.