
Dr Anne-Quillet-Mary
Résistance Des Cellules Leucémiques Et Immunitaires Aux Thérapies Ciblées Dans La Leucémie Lymphoïde Chronique (LLC)
La leucémie lymphoïde chronique (LLC) est la deuxième forme la plus fréquente des lymphomes B non-Hodgkiniens. Cette pathologie est caractérisée par une survie/prolifération, dépendante du microenvironnement des cellules LLC dans les organes lymphoïdes secondaires et l’accumulation de lymphocytes B leucémiques quiescents dans le sang.
La prise en charge clinique des patients en première ligne ou en rechute, a été révolutionnée par le développement de thérapies ciblées, administrées par voie orale, notamment l’ibrutinib (inhibiteur de BTK, Bruton Tyrosine Kinase), et le venetoclax (inhibiteur de BCL-2) en association ou non avec les anticorps thérapeutiques anti-CD20. Malgré de longues durées de rémission, 2 mécanismes de résistance se développent toujours : sélection clonale avec mutations acquises des gènes BTK/PLCg2 et BCL2, ou transformation brutale (imprévisible, indépendante des mutations précitées) en lymphome agressif (syndrome de Richter, RT). Dans une cohorte prospective longitudinale de patients traités par ibrutinib en monothérapie, nos résultats montrent que seuls 60% des patients en progression sous traitement (> 3 ans d’ibrutinib) ont acquis une de ces 3 mutations pouvant rendre compte de la rechute. Cette étude témoigne de la grande variété des altérations génomiques permettant la résistance à l’ibrutinib. Néanmoins, au niveau cellulaire, les programmes transcriptomiques régulés par ces mutations ne sont pas identifiés.
Objectifs du projet de recherche :
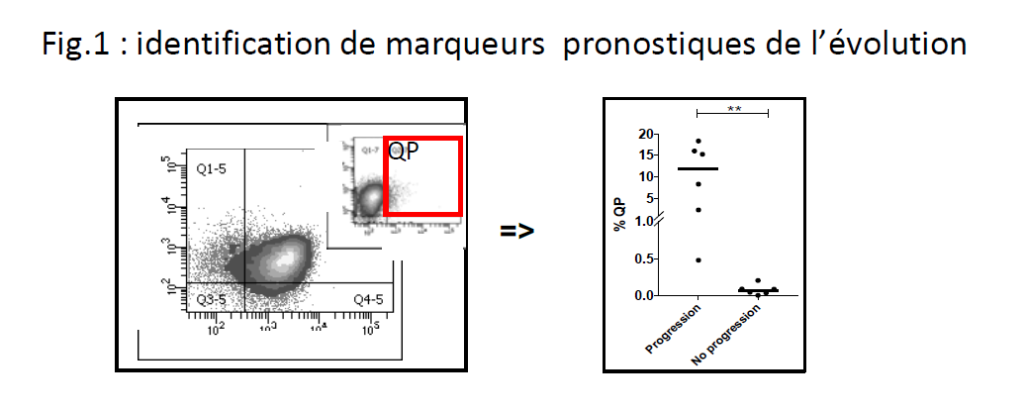
- identifier des marqueurs pronostiques de l’évolution des patients LLC sous thérapies ciblées pour mieux anticiper la progression ou la transformation
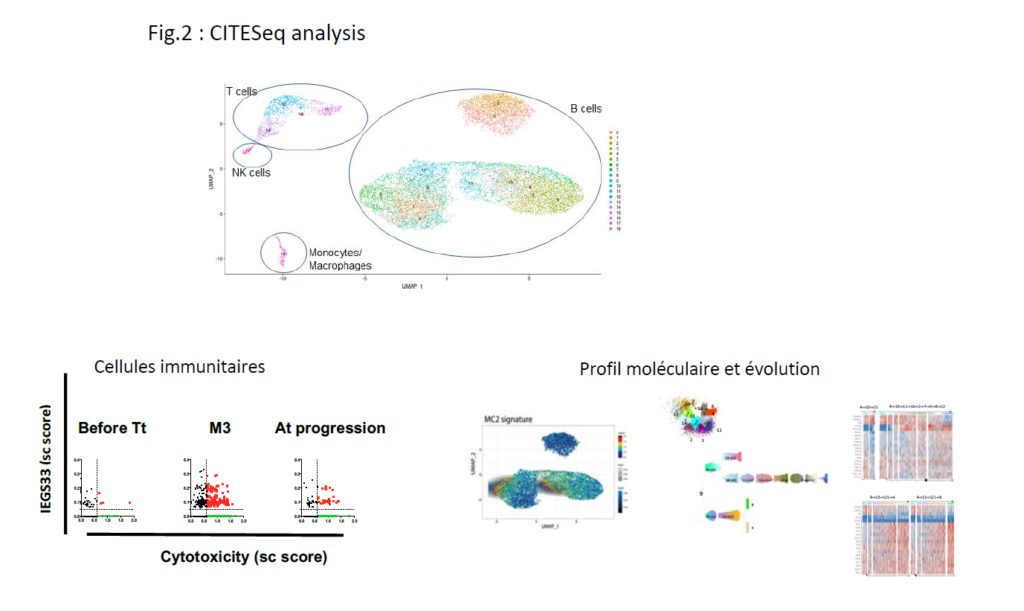
- par une approche de haute technologie de séquençage sur cellule unique (CITESeq) : comprendre l’état physiologique des cellules immunitaires normales, identifier la signature génétique des cellules leucémiques résistantes et définir de nouvelles cibles thérapeutiques
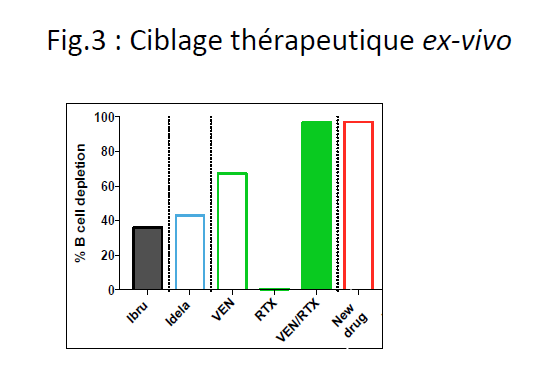
- valider les cibles identifiées par CITESeq par criblage thérapeutique ex-vivo et proposer le traitement le plus adapté à chaque cas
Partenaires et Financeurs :
IUC/CRCT (Projet Demetar ; AO Translationnel)

