Équipe
Julie Guillermet-Guibert
SigDYN :
Signalisation cellulaire intégrée et isoformes de PI3K

Les spécificités
de notre axe de recherche
La famille des kinases lipidiques appelées phosphoinositide 3-kinases (PI3K) est impliquée dans des fonctions cellulaires majeures telles que la survie, la prolifération, la croissance, la migration, la différenciation cellulaire mais aussi la synthèse des protéines et le trafic vésiculaire intracellulaire. Chez les vertébrés, la famille PI3K est divisée en trois classes différentes. Cette classification est basée sur leur structure, leur mode d’activation et la spécificité de leur substrat lipidique in vitro et in vivo. Ces enzymes, codées par 8 gènes différents, phosphorylent le groupement hydroxyle en position 3 du noyau inositol des phosphoinositides, d’où leur nom.
Seule, la classe I (composée de PI3Kα, PI3Kβ, PI3Kγ, PI3Kδ) peut produire à partir du phosphatidylinositol (4,5) -bisphosphate [PtdIns-4,5-P2, PtdIns (4,5) P2, PIP2] du phosphatidylinositol (3,4,5) -trisphosphate [PtdIns-3,4,5-P3, PtdIns (3,4,5) P3, PIP3]. Le substrat des enzymes de classe I est majoritairement localisé à la membrane cellulaire. Ainsi, l’activation des PI3K de classe I produit un second messager lipidique à la membrane plasmique à l’interface avec le cytoplasme, ce qui permet la transmission de l’information biochimique dans le cytoplasme et qui conduit à une réponse cellulaire.
Les PI3K de classe II (PI3KC2α, PI3KC2β, PI3KC2γ) et de classe III (VPS34) peuvent générer du phosphatidylinositol 3-phosphate [PtdIns-3-P, PtdIns (3) P, PI-3-P]. Les PI3K de classe II peuvent aussi synthétiser le phosphatidylinositol (3,4) -bisphosphate [PtdIns-3, 4-P2, PtdIns (3,4) P2]. Les substrats de ces enzymes sont présents dans les membranes externes des organites à l’intérieur de la cellule, au niveau des endosomes, des autophagosomes. Ainsi, les PI3K de classe II et III contrôlent le trafic vésiculaire intracellulaire.
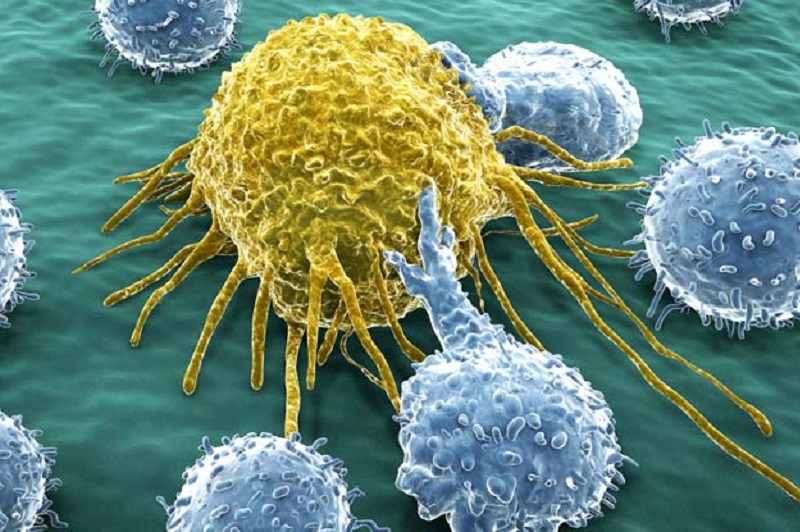
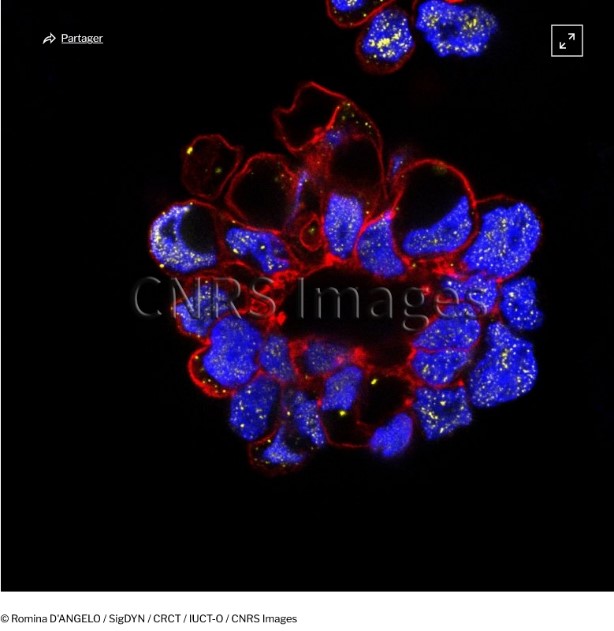
La forte activation des PI3K de classe I est considérée comme une caractéristique du cancer ; cependant, le rôle de chaque PI3K de classe I dans les différentes étapes de cancérogenèse est mal connu. Ces recherches sont réalisées par notre équipe.
Les rôles des PI3K de classe II et III dans le cancer sont très peu étudiés. Nous avons entrepris de les comprendre.
Signalisation oncogénique
PI3K
thérapies ciblées
résistance
niche tumorale
initiation du cancer
mécanobiologie
compression
souris génétiquement modifiées
imagerie des tumeurs
cancer du pancréas
cancer de l’ovaire
DES PROJETS
DE RECHERCHE
Mieux diagnostiquer et traiter avec les thérapies ciblées.
Dr C.Basset
Importance des isoformes de PI3K en physiopathologie
Dr B.Thibault
Importance des isoformes de PI3K comme intégrateur majeur de la mécanotransduction.
Dr M.Delarue et Dr M.Di-Luoffo
LES FOCUS
DE L’ÉQUIPE
Découvrir
Comprendre
Participer
PRODUCTIONS SCIENTIFIQUES
PUBLICATIONS 2024
PUBLICATIONS 2023
PUBLICATIONS 2022
PUBLICATIONS 2021
PUBLICATIONS 2020
PUBLICATIONS 2019
LES MEMBRES DE L’ÉQUIPE
LES PARTENAIRES & FINANCIERS

Centre de Recherches en Cancérologie de Toulouse (Oncopole)
Toulouse – FR
Nous contacter
05 82 74 15 75
Envie de rejoindre
L’équipe du CRCT ?